Võ Hữu Công1, Nguyễn Thanh Lâm1, Đinh Thị Hải Vân1,
Trần Đức Viên2 và Yutaka Sakakibara3
1Bộ môn Quản lý Môi trường,
Học viện Nông nghiệp Việt Nam, Hà Nội
Email: vhcong@vnua.edu.vn
2Trung tâm Sinh thái Nông nghiệp,
Học viện Nông nghiệp Việt Nam, Hà Nội
Email: tdvien@cares.org.vn
3Department of Civil and Environmental Engineering,
Waseda Univeirsity, Japan
Email: sakaki@waseda.jp
Tóm tắt
Xử lý các chất vết hữu cơ trong nước thải gặp nhiều khó khăn vì nó có độc tính cao dù ở nồng độ rất nhỏ. Trong thực tế, đã có nhiều phương pháp xử lý nhưng hiệu quả xử lý không cao hoặc tạo ra sản phẩm phụ có độc tính mạnh. Bài báo này trình bày tiếp cận mới của công nghệ điện hoá để xử lý chất thải vết hữu cơ trong nước thải. Các thí nghiệm được thực hiện nhằm đánh giá một số điều kiện cơ bản và hiệu quả xử lý đối với các chất rối loạn nội tiết bằng sử dụng hệ thống điện cực carbon hoạt tính. Kết quả cho thấy quá trình oxi hoá có thể thực hiện ở dải pH 3-10 ở mức điện thế từ 0.5-0.8V. Mức độ xử lý đạt trên 80% tại điện thế 1.0V. So sánh với một số nghiên cứu cùng loạicho thấy tiêu hao năng lượng thấp hơn 1000 lần. Tuy nhiên, để có thể áp dụng công nghệ này vào thực tiễn, nghiên cứu về sử dụng các loại vật liệu có thể sản xuất carbon hoạt tính nên được thực hiện.
Từ khoá: chất rối loạn nội tiết, điện hoá, điện cực, nước thải, than hoạt tính
Summary
This paper summaries an examination of operating conditions for electro-chemical oxidation of trace endocrine disrupting chemicals in synthetic wastewater containing estradiol (E2) and 2,4 dichlorophenol (DCP). The results show that although E2 and DCP oxidized in the range of 0.5-0.8V, the optimal condition for electropolimerization is achieved in alkaline condition. In addition, the continous treatments show that more than 80% of removal efficiency was achived with an energy consumption around 1-10 Wh/m3. It is recommended that further studies using existing material at the local site shoud be conducted to make this process possile in practice.
Keywords: electrochemical, endocrine disrupting chemical, electrode, activated carbon, wastewater
I. ĐẶT VẤN ĐỀ
Nghiên cứu về ảnh hưởng và xử lý các chất gây rối loạn nội tiết “endocrine disrupting chemicals-EDCs” trong môi trường khá mới mẻ ở Việt Nam. Tuy nhiên, đã có nhiều nghiên cứu trên thế giới tập trung vào các nghiên cứu đánh giá độc tố của các chất này đối với các loài động thực vật thuỷ sinh, cũng như con người. Theo Tổ chức Y tế thế giới (WHO, 2012) thì EDCs là các chất có mặt trong thành phần của thuốc thừ sâu, kim loại, phụ gia và trong thức ăn hoặc các sản phẩm làm đẹp. Viện nghiên cứu quốc gia về khoa học sức khoẻ môi trường (NIEHS, 2015) nhấn mạnh rằng EDCs là những chất có thể can thiệp vào hệ thống nội tiết của cơ thể và tạo ra những ảnh hưởng đến sự phát triển, sinh sản, thần kinh và hệ thống miễn dịch của cả con người và động vật. Ngoài các chất do WHO liệt kê, NIEHS còn đề cập đến các chất thải trong y tế, dioxin và các chất có hoạt tính của dioxin, polychlorinated biphenyls, các thành phần của nhựa như bisphenol A.Đến tháng 7 năm 2015, Tổ chức bảo vệ môi trường Mỹ (US. EPA, 2015) đã chính thức công bố 52 hoá chất gây rối loạn nội tiết.
Ở Việt nam, Dương N. Cường và cộng sự (2010) đã công bố nồng độ của một số EDCs như nonyl phenol (NP), octyl phenol (OP), bisphenol A (BPA), estron (E1), 17β-estradiol (E2), và 17α-Ethynylestradiol (EE2) trong nước sông. Trong các chất trên, E2 và EE2 là những chất có hoạt tính mạnh nhất và có giá trị cao nhất so với các nước trong khu vực như Lào, Campuchia, Thái Lan, Indonesia và Trung Quốc.Số lượng các chất gây hại được xác định tăng lên khi Dương Thị Hạnh và cộng sự (2014) công bố 940 chất hữu cơ gây ô nhiễm từ lớp trầm tích của một số con sông xuất phát từ các thành phố lớn. Kết quả này cũng cho thấy nhiều chất rối loạn nội tiết có nguồn gốc từ nước thải sinh hoạt.
Việc xử lý nước thải có chứa các chất gây rối loạn nội tiết đã được thực hiện bằng nhiều phương pháp như màng sinh học (MBR) (Meang và cộng sự, 2013; Trinh và cộng sự, 2012; Zhou và cộng sự, 2011), bùn hoạt tính (activated sludge) (Li và cộng sự, 2010), lọc hấp phụ và sử dụng emzym (Tanaka và cộng sự, 2009; Reis và Sakakibara, 2012). Các phương pháp này cho thấy ưu thế khi xử lý các chất thải có nồng độ cao.Tuy nhiên, điều kiện để đạt hiệu quả tối ưu rất khắt khe và phụ thuộc vào độ pH, nhiệt độ hoặc thời gian tiếp xúc với chất thải. Phương pháp xử lý áp dụng chu trình oxy hoá tiên tiến (AOP) đã cho thấy nhiều tiến bộ trong việc xử lý triệt để các chất thải và thường được áp dụng như là bước cuối cùng trước khi thải ra môi trường (Sakakibara và cộng sự, 2010;Fengvà cộng sự, 2010). Trong đó, phương pháp điện hoá là biện pháp hàng đầu dựa vào khả năng tạo ra gốc tự do ·OH để phá vỡ các cấu trúc hoá học của thành phần chất hữu cơ (Anglada và cộng sự, 2009). Do đặc thù của nước thải chứa các hàm lượng chất hữu cơ khác nhau, phương pháp này tiêu tốn khá nhiều điện năng do các gốc ·OH được tạo ra đều phản ứng và phá vỡ các thành phần có trong nước thải (Công và cộng sự, 2014).
Trong nước thải sinh hoạt, các chất gây rối loạn nội tiết thường tồn tại ở một nồng độ rất nhỏ (nanogram/lít đến microgram/lít) nhưng tính độc rất cao và được gọi là chất vết hữu cơ. Do cấu tạo có gốc phenol, giả thiết đặt ra là các chất này có thể polymer hoá trên điện cực anốt. Để xử lý hiệu quả hoạt chất này, chúng tôi đã sử dụng nguồn vật liệu carbon hoạt tính làm điện cực hoạt động nhằm tăng khả năng tiếp xúc của chất vết hữu cơ trong nước và điện cực thông qua quá trình polyme hoá. Đây là một tiếp cận hoàn toàn mới trong việc xử lý các EDCs nhằm giảm thiểu phát sinh ra môi trường. Theo Công và Sakakibara (2015), quá trình polymer hoá đã được thực hiện thành công trên điện cực Platinium và đạt hiệu quả xử lý trên 92%. Tuy nhiên, việc sử dụng vật liệu trên vào thực tiễn ởViệt Nam sẽ không khả thi vì chi phí cho điện cực vô cùng tốn kém. Do đó, trong nghiên cứu này, chúng tôi thử nghiệm các vật liệu carbon hoạt tính nhằmtìm hiểu khả năng ứng dụng của nó trong việc xử lý nước thải có chứa các EDCs.
II. NỘI DUNG NGHIÊN CỨU
2.1 Đối tượng nghiên cứu
Đối tượng nghiên cứu là vật liệu carbon hoạt tính trong các quy trình điện hoá để loại bỏ các chất gây rối loạn nội tiết.
Phạm vi nghiên cứu tập trung vào khả năng thực hiện các phản ứng bề mặt trên các điện cực ở các điều kiện hoạt động khác nhau như: ảnh hưởng của nồng độ ban đầu, các giá trị pH ở điều kiện axit, trung tính và kiềm, nhịp quét điện thế. Nghiên cứu thử nghiệm trên đối tượng chính là 17β-estradiol (E2) và 2,4 dichorophenol (DCP hoặc 2,4D) vì đây là hai trong số EDCs có độc tính mạnh và phổ biến trong môi trường.
2.2 Phương pháp nghiên cứu
2.2.1 Vật liệu nghiên cứu
Hoá chất: 17β-Estradiol và 2,4 dichorophenol tiêu chuẩn có độ tinh khiết trên 98% được mua từ công ty hoá chất Wako Nhật Bản. Các dung dịch gốc (1 mg/mL) được chuẩn bị bằng cách pha 10 mg từng chất trên vào 10 mL Acetone (độ tinh khiết đạt tiêu chuẩn phân tích PCB). Các dung dịch gốc được cất giữ trong tủ lạnh ở 0℃ và pha với nước tuỳ vào điều kiện của từng thí nghiệm.
Điện cực : Trong nghiên cứu này, chúng tôi sử dụng hai hệ thống điện hoá để đánh giá khả năng xử lý của các bộ phận, trong đó 1) nghiên cứu cơ bản về phản ứng của các chất trên bề mặt điện cực bằng hệ thống quét điện liên hồi (cyclic voltammetry-CV) cho hạt và sợi carbon hoạt tính và 2) hệ thống thực nghiệm xử lý E2 và DCP sử dụng sợi carbon.
2.2.2 Thiết kế thí nghiệm
Hệ thống phân tích CV cấu tạo, gồm 1 điện cực hoạt động glassy carbon (anốt) nối với 1 sợi Platinum (ca thốt) và điện cực tham chiếu Ag/AgCl. Tổng thể tích thí nghiệm là 20 mL. Sau mỗi thí nghiệm, các điện cực được làm sạch và đánh bóng bằng bộ PK-3 chứa các hạt kim cương thô 1μm (Cat.No. 012621) và dung dịch đánh bóng nhôm 0.05 μm (Cat.No. 012620). Các thiết bị này được mua từ công ty BAS Inc., Nhật Bản. Hệ thống phân tích CV được nối với mô đun điều khiển HZ-5000 (Hokuto Electronic Inc.).
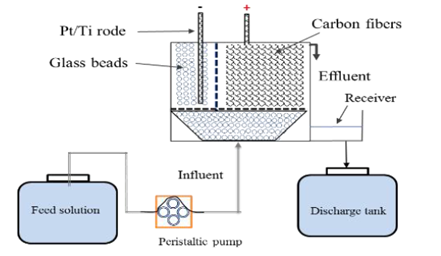
Hệ thống thực nghiệm xử lý liên tục, gồm 2 khoang bên trong chứa các sợi carbon ở a nốt và miếng Platinum mạ Titanium (Pt/Ti) ca thốt. Tổng diện tích bề mặt của sợi carbon là 2000 cm2 và thể tích là 50 mL. Trong thí nghiệm liên tục, nước thải tự tạo có chứa E2 và DCP được cung cấp liên tục cho hệ thống xử lý bằng một bơm điều hoà với thời gian lưu là 15 phút (Hình 1). Hiệu suất xử lý được đánh giá thông qua chênh lệch của nồng độ đầu ra so với đầu vào ở các hiệu điện thế là 0.5, 1.0, 2.0 và 3.0 V.
Hình 1. Sơ đồ hệ thống xử lý nước thải chứa E2 và DCP
2.2.3 Lấy mẫu và phân tích
Các mẫu được xử lý và phân tích ngày sau khi lấy lấy ra từ hệ thống. Phương pháp lấy mẫu đã được mô tả cụ thể trong Công và Sakakibara (2015). Tuy nhiên, các điểm cần chú ý trong công tác lấy mẫu là các mẫu phải được lọc qua một lớp màng có các lỗ có kích thước 0.45 μm (Advance Tech) nhằm loại bỏ các hạt lơ lửng hoặc các tạp chất có trong mẫu. Các mẫu này được cố định bởi 10 μL E2-d3 có nồng độ chuẩn sau điều chế là 100μg/L để hiệu đính sai số.Quy trình tách và chiết các chất E2 và DCP trong nước được thực hiện theo phương pháp Liquid-Liquid extraction. Các mẫu sẽ được trộn với ethylacetate trước khi dùng máy lắc ở 260 nhịp/phút để tách E2 và DCPra khỏi mẫu nước. Các mẫu được cho vào các lọ nhỏ (vial) sau đó thêm các chất hoạt hoá như pyridine, BSTFA trước khi phân tích. Quá trình phân tích nồng độ E2 và DCP được thực hiện bằng máy phân tích sắc ký khí khối phổ (GC/MS) Shimadzu QP5050, Nhật Bản.
2.3.4 Đánh giá hiệu quả xử lý
Hiệu quả xử lý (RE) được tính dựa vào công thức sau (1).
Trong đó, Cinf và Ceff là nồng độ đầu vào và nồng độ đầu ra tai thời điểm t.
III. KẾT QUẢ NGHIÊN CỨU VÀ THẢO LUẬN
3.1. Ảnh hưởng của các điều kiện hoạt động
3.1.1 Nồng độ ban đầu (C0)
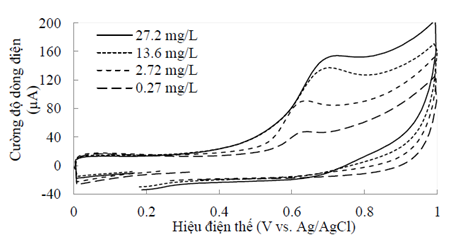
Trong môi trường nước chứa chất hữu cơ dễ bị oxi hoá, khi hiệu điện thế giữa 2 điện cực tăng đều thì tại một ngưỡng xác định, quá trình oxi hoá sẽ xảy ra. Quá trình đánh giá các phản ứng oxi hoá trên bề mặt điện cực carbon được thực hiện ở pH trung tính 6,5-7,0.Phản ứng điện hoá đối với các nồng độ ban đầu là 0,27; 2,7; 13,6và 27,2 mg/L E2 được đánh giá trên điện cực carbon hoạt tính với nhịp quét (scan rate) ở 100 mV/s. Hình 2 cho thấy các điểm cực đại (peak) của cường độ dòng điện chứng tỏ quá trình oxi hoá của E2 xảy ra trong khoảng 0,5V-0,8V. Đây là ngưỡng điện thế thấp hơn giá trị thuỷ phân của nước (E=1.7V) (Chen, 2004). Kết quả này cho thấy việc loại bỏ E2 ra khỏi môi trường nước có tính chất chọn lọc. Tức là, khi áp dụng một hiệu điện thế giữa 2 điện cực thì điện năng chỉ dùng cho việc loại bỏ E2, không tiêu hao cho việc phân huỷ các thành phần khác trong nước.
Khi nồng độ ban đầu của E2 tăng lên 10 lần thì cường độ dòng điện có xu hướng tăng gấp đôi.Điều này chứng tỏ rằng quá trình oxi hoá E2 tuân theo quy luật chuyển khối (mass transfer) từ pha lỏng lên điện cực (Wilson và Geankoplis, 1966).Mặt khác, kết quả nghiên cứu cho thấy điện cực carbon hoạt tính có thể sử dụng cho việc xử lý chất thải có nồng độ khá cao lên đến 27 mg/L.
Hình 2. Phản ứng oxi hoá của E2 trên bề mặt điện cực carbon hoạt tính
3.1.2 Điều kiện pH
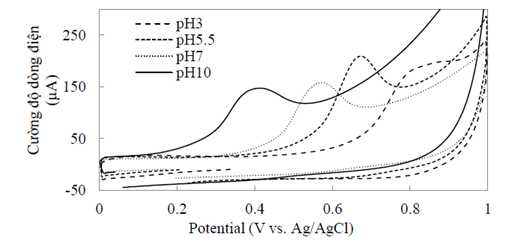
Nghiên cứu về ảnh hưởng của pH được thực hiện đối với 3 loại estrogens là estrone (E1), estradiol (E2) và 17α-ethynylestradiol (EE2) ở cùng nồng độ ban đầu là 2,72 mg/L trong dung dịch đệm phosphate. Bên cạnh điều kiện nồng độ ban đầu, giá trị pH trong môi trường nước có ảnh hưởng rất lớn đến oxi hoá của các estrogen. Hình 3 thể hiện các phản ứng oxi hoá của EE2 ở các ngưỡng: a xít (pH 3.0-5.5), trung tính (pH ~7.0) và kiềm (pH 10). Qua hình 3 cho thấy, các estrogen có thể bị oxi hoá ở tất cả các điều kiện pH từ axit đến kiềm. Đây là yếu tố thuận lợi cho việc áp dụng công nghệ điện hoá xử lý nước thải ở trong các điều kiện khác nhau mà các quy trình ứng dụng các yếu tố sinh học không hiệu quả.
Qua quan sát cho thấy, ở điều kiện môi trường kiềm (pH 10), các estrogen dễ bị oxi hoá ở điều kiện hiệu điện thế thấp. Theo tính chất vật lý, các estrogen này có pKa 10.2-10.4, nênkhi trong môi trường có pH 10 cả ba estrogen này dễ bị ion hoá. Khi mất proton H+, các estrogen này tồn tại ở dạng anion (tích âm) nên di chuyển về điện cực anot. Trong một nghiên cứu tương tự, Tahar và Saval (2011) đã công bố quá trình polymer hoá sản phẩm BPA trên điện cực carbon hoạt tính. Nghiên cứu này, chúng tôi chứng minh rằng xử lý estrogen trong môi trường nước có thể thực áp dụng quá trình polymer hoá. Ở pH trung tính (pH 7.0), quá trình oxi hoá cũng diễn ra ở mức hiệu điện thế 0.6V. Do vậy, trong các thí nghiệm thử nghiệm với các loại nước thải tự tạo, chúng tôi sử dụng ngưỡng pH từ 6.0-7.0.
Hình 3. Oxi hoá EE2 trên điện cực carbon hoạt tính ở các pH khác nhau
3.1.3 Nhịp quét (Scan rates)
Nhịp quét là một trong số yếu tố rất quan trọng trong phân tích CV. Nhịp quét thường được tính bằng hiệu điện thế trên một đơn vị thời gian (mV/s).Theo lý thuyết, cường độ dòng điện từ quá trình oxi hoá tỷ lệ thuận với căn bậc hai của dải quét.Trong nghiên cứu này, phương trình Randles-Sevcik được sử dụng để so sánh số liệu thực nghiệm so với các lý thuyết. Giả thiết đưa ra là quá trình oxi hoá các estrogen thông qua quá trình polymer hoá nên 2 electron sẽ trao đổi trên điện cực anot.Ảnh hưởng của nhịp quét (v) đến cường độ dòng điện(ip)được thể hiện qua công thức (2) (Bard and Faulkner, 1944):
ipf= (2.69 x 105) n3/2 AD 1/2C*v1/2 (2)
Trong đó, nlà số điện tích (electron) trao đổi trong quá trính polymer hoá; A (cm2) là diện tích hữu dụng của anot; D (cm2/s) là hệ số khuếch tán; C* (mol/cm3) là nồng độ của các estrogen trong nước; vlà nhịp quét (V/s). Trong nghiên cứu này, n =2; A = 10 cm2, DE1 = 0.54 x 10-5 cm2/s; DE2 = 0.52 x 10-5 cm2/s; DEE2 = 0.51 x 10-5 cm2/s; C* = 10-5 mol/cm3, v = 0.01 đến 1.0 V/s.
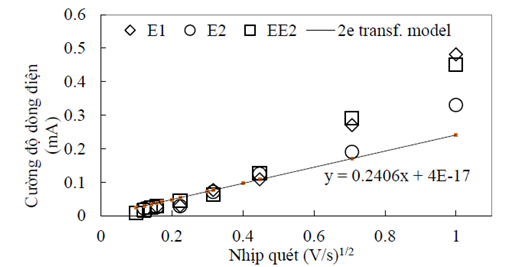
Hình 4 thể hiện mức độ oxi hoá của E1, E2 và EE2 trên điện cực carbon hoạt tínhtại các nhịp quét khác nhau. Đối với mỗi chất, quá trình oxi hoá tỷ lệ thuận với nhịp quét. So sánh với công thức lý thuyết, oxi hoá của các chất này có quan hệ chặt với nhịp quét dưới 250 mV/s. Tuy nhiên, khi nhịp quét cao hơn 500 mV/s thì cường độ dòng điện tăng đột biến. Đây có thể là kết quả của sử thuỷ phân hoặc trao đổi các phần tử hoạt động có trong dung dịch.
Hình 4. Ảnh hưởng của nhịp quét đến cường độ dòng điện oxi hoá. Điều kiện thí nghiệm điển giải 10 mmol/L Na2SO4; Nồng độ E1, E2, EE2: 0.01 mmol/L
3.2 Hiệu quả xử lý E2 và DCP
3.2.1 Kết quả thí nghiệm liên tục
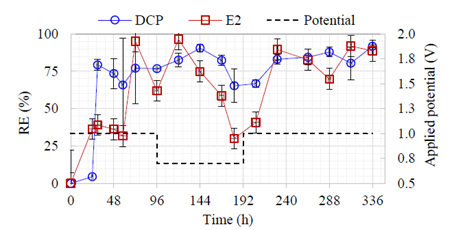
Để đánh giá khả năng ứng dụng vào thực tiễn, thí nghiệm xử lý liên tục được thực hiện trong thời gian 14 ngày. Khác với các thí nghiệm trước đó (Sakakibara và cộng sự, 2010, Công và cộng sự, 2014), E2 và DCP được trộn lẫn với nồng độ ban đầu mỗi chất là 100 μg/L. Quá trình loại bỏ hỗn hợp 2 chất trên được thực hiện trong các điều kiện hiệu điện thế khác nhau (1.0V, 0.5V và 1.0V) (Hình 5).
Kết quả cho thấy, khi kết nối hai điện cực với hiệu điện thế 1.0V, hiệu quả xử lý E2 và DCP đạt 60% trong 20 giờ. Tuy nhiên, ở giai đoạn này, hiệu quả xử lý đạt được không ổn định do hệ thống xử lý chưa đạt được trạng thái bão hoà. Để đánh giá độ nhạy của hệ thống xử lý, hiệu điện thế được thiết lập tại 0.5V ở dưới mức cực đại của oxi hoá (theo kết quả mục 3.1). Kết quả đạt được phản ánh đúng giả thiết rằng quá trình loại bỏ E2 và DCP được thực hiện thông qua quá trình polymer hoá. Khi giá trị hiệu điện thế được điều chỉnh quay về 1.0V, hiệu quả xử lý đạt trên 80% và bắt đầu đạt được sự ổn định. Đây là kết quả ban đầu trong việc áp dụng hệ thống xử lý tích hợp các điện cực carbon hoạt tính trong xử lý các chất vết hữu cơ. Để đưa hệ thống này vào thực tiễn xử lý nước thải ở Việt Nam, các nghiên cứu sâu hơn nên tập trung vào việc sử dụng da dạng vật liệu từ nguồn gốc tự nhiên, sẵn có ở địa phương. Ngoài ra, đánh giá hiệu quả xử lý cũng như thời gian hữu hiệu cho việc xử lý các chất thải khác nhau.
Hình 5. Hiệu quả xử lý liên tục hỗn hợp DCP và E2 bằng hệ thống tích hợp điện cực sợi carbon ở các hiệu điện thế khác nhau.
3.2.2 Đánh giá hiệu suất xử lý
Mức độ tiêu hao năng lượng cho việc xử lý nước thải được tính dựa vào số liệu thực nghiệm từ thí nghiệm xử lý liên tục đối với nồng độ 100 μg/L E2 và DCP. Hình 6 thể hiện mức tiêu thụ năng lượng trong nghiên cứu này so với các nghiên cứu cùng chủ đề khác. Kết quả cho thấy, khi áp dụng quá trình xử lý nước thải có chứa các chất vết gây rối loạn nội tiết, mức độ tiêu hao năng lượng ở mức 1-10 Wh/m3 nước thải được xử lý.
Hình 6. Năng lượng tiêu thụ của quá trình xử lý E2 và DCP
KẾT LUẬN
Quá trình oxi hoá của các estrogen xảy ra trong khoảng từ 0,5 – 0,8V và không phụ thuộc vào nồng độ ban đầu. Tuy nhiên, nồng độ ban đầu càng tăng thì khả năng oxi hoá cũng tăng. Môi trường kiềm (ở mức pH 10) thuận lợi cho quá trình oxi hoá của các estrogen. Trong thí nghiệm thực nghiệm xử lý liên tục E2 và DCP, hiệu quả xử lý đạt 87%-91%. Qua đó, chúng tôi đề xuất nghiên cứu thêm trên các đối tượng điện cực carbon hoạt tính có sẵn trong tự nhiên để giảm chi phí và có khả năng đưa vào thực tiễn.
Lời cảm ơn
Tác giả xin cảm ơn sự hỗ trợ một phần tài chính từ quỹ Grant-in-Aid for Scientific Research (B) tại Sakakibara Lab., ĐH Waseda (No. 24360219), MEXT, Nhật Bản.
TÀI LIỆU THAM KHẢO
- Anglada, A., Urtiaga, A. and Ortiz, I. Contributions of electrochemical oxidation to wastewater treatment: fundamentals and review of applications. Journal of Chemical Technology and Biotechnology 84(12), 1747–1755, 2009.
- Bard, J.A. và Faulkner, R.L,. Electrochemical Methods: Fundamentals and Applications, John Wiley & Sons, 1980, USA.
- Chen, G.,. Electrochemical technologies in wastewater treatment. Separation and Purification Technology 38 (1), 11–41, 2004.
- Cong,VH. và Sakakibara,Y,. Electrolytic Treatment of Trace Natural and Synthetic Estrogens. Journal of Advanced Oxidation Technologies 17 (1), 115–120, 2014.
- Cong, VH. và Sakakibara Y., Continuous treatments of estrogens through polymerization andregeneration of electrolytic cells. Journal of Hazardous Materials 285, 304–310, 2015.
- Cong, VH., Iwaya, S., và Sakakibara, Y.,. Removal of estrogens by electrochemical oxidation process. Journal of Environmental Sciences 26, 1355–1360, 2014.
- Duong, CN., Ra, JS., Cho, J.Kim, SD.Choi, HK.Park, JH.Kim, KW. Inam, E., và Kim, SD. Estrogenic chemicals and estrogenicity in river waters of South Korea and seven Asian countries. Chemosphere 78(3):286-93, 2010.
- Duong, HT, Kadokami, K, Pan, S, Matsuura, N, và Nguyen, TQ. Screening and analysis of 940 organic micro-pollutants in river sediments in Vietnam using an automated identification and quantification database system for GC-MS. Chemosphere 107, 462-72, 2014.
- Feng, Y., Wang, C., Liu, J. và Zhang, Z.,. Electrochemical degradation of 17-alpha-ethinylestradiol (EE2) and estrogenic activity changes. Journal of Environmental Monitoring 12, 404-408, 2010.
- Li, Y.M., Zeng, Q.L. và Yang, S.J., Removal and fate of estrogens in an anaerobic-anoxic-oxic activated sludge system. Water Science and Technology 63 (1), 51-56, 2010.
- Maeng, S.K., Choi, B.G., Lee, K.T. và Song, K.G.,. Influences of solid retention time, nitrification and microbial activity on the attenuation of pharmaceuticals and estrogens in membrane bioreactors. Water Research 47 (9), 3151-3162, 2013.
- Murugananthan, M., Yoshihara, S., Rakuma, T., Uehara, N. và Shirakashi, T. Electrochemical degradation of 17β-estradiol (E2) at boron-doped diamond (Si/BDD) thin film electrode. Electrochimica Acta 52, 3242-3249, 2007.
- Reis, A.R. và Sakakibara, Y., Enzymatic degradation of endocrine-disrupting chemicals in aquatic plants and relations to biological Fenton reaction. Water Science and Technology 66(4), 775-782, 2012.
- Sakakibara, Y., Kounoike, T. và Kashimura, H., 2010. Enhanced Treatment of Estrogen and Endocrine Disrupting Chemicals (EDCs) by A Granular Bed Electrochemical Reactor. Water Science and Technology 62, 2218-2224.
- Sarkar, S., Ali, S., Rehmann, L., Nakhla, G. và Ray, MB., Degradation of estrone in water and wastewater by various advanced oxidation processes. Journal of Hazardous Materials 278, 16-24. 2014.
- Tahar, N.B. và Savall, A.. Electropolymerization of phenol on a vitreous carbon electrode in alkaline aqueous solution at different temperature. Electrochimica Acta 55, 465-469, 2011.
- Tanaka, T., Tamura, T., Ishizaki, Y., Kawasaki, A., Kawase, T., Teraguchi, M. và Taniguchi, M.,. Enzymatic treatment of estrogens and estrogen glucuronide. Journal of Environmental Sciences 21, 731-735, 2009.
- Trinh, T., van den Akker, B., Stuetz, R.M., Coleman, H.M., Le-Clech, P. và Khan, S.J., Removal of trace organic chemical contaminants by a membrane bioreactor. Water Science and Technology 66(9), 1856-1863, 2012. .
- US. EPA, Endocrine Disruptor Screening Program (EDSP). Truy cập ngày 23/8/2015. http://www2.epa.gov/ingredients-used-pesticide-products/endocrine-disruptor-screening-program-tier-1-assessments, 2015..
- Wilson E.J. và Geankopolis C.J.,. Liquid mass transfer at very low Renolds numbers in packed beds. I&EC Fundamentals 5, 9-14, 1966.
- World Health Organizations (WHO). Endocrine Disrupting Chemicals. Truy cập ngày 23/8/2015. http://www.who.int/ceh/risks/cehemerging2/en/, 2012.
- Zhou, Y., Huang, X., Zhou, H., Chen, J. và Xue, W. Removal of typical endocrine disrupting chemicals by membrane bioreactor: in comparison with sequencing batch reactor. Water Science and Technology 64(10), 2096-2102, 2011.
………………………………………………………………………………….
Nguồn: Trích dẫn từ kỷ yếu Hội nghị môi trường toàn quốc lần thứ IV, Bộ tài nguyên và Môi trường, Hà Nội, 29/09/2015
…………………………………………………………………………………..

Leave a Reply